基于邻近效应诱导的DNA自组装是构建快速、免洗脱的蛋白检测传感器的基本原理之一,被广泛应用于超灵敏蛋白检测与原位成像。然而,当前设计策略普遍存在识别亲和力与检测背景之间的内在制约,这是由于较长的DNA互补序列可以通过多价识别提升传感器的亲和力,但会造成过高的背景信号。如何在不增加背景的前提下,提升蛋白识别的亲和力仍然是本领域的一个重要挑战。
近日,四川大学李峰教授团队提出利用组分动态化学解决基于邻近诱导DNA组装的蛋白传感器设计的内在制约。不同于仅包含两个探针的传统设计方案,本策略包含4个可以可逆组装的探针组分,从而构成组分动态网络。通过精细调控组分中激动剂与拮抗剂的比例,实现了在最大限度提高对目标蛋白质亲和力的同时,将导致背景信号的非特异性相互作用降至最低。通过对可逆的动态平衡的精细调控,所开发传感器还可以显著提高检测方法的稳健性,从而能够血清等复杂基质中灵敏地检测抗体。凭借高亲和力、低背景和高稳健性的特点,该工作展示了组合动态化学在生物传感器设计中的巨大潜力。
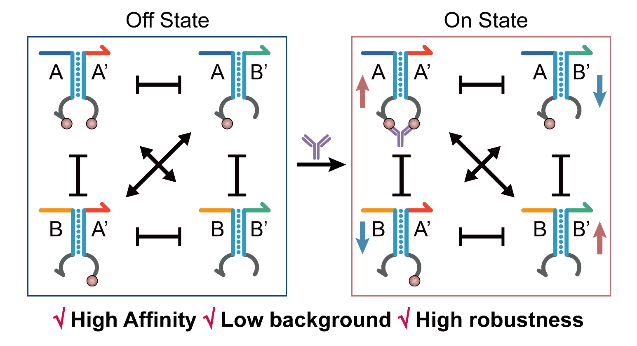
图1.基于组分动态化学的蛋白传感器构筑策略
该工作以题为“Engineering a Proximity Biosensor via Constitutional Dynamic Chemistry”发表于《Angewandte Chemie International Edition》。论文第一作者是四川大学化学学院博士研究生高露(现为上海交通大学博士后)和硕士研究生张瑞琪,通讯作者为四川大学化学学院李峰教授和分析测试中心的唐娅楠副研究员。以上工作得到科技部、国家自然基金委的经费支持。
文章链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202425644
